Funkce tlumivého roztoku
Tlumivý roztok nebo‑li pufr je obecně známý tím, že dokáže udržet stabilní pH. O jeho funkčnosti se lze přesvědčit měřením pH, po přidání kyseliny či zásady, pomocí skleněné kombinované elektrody. Tenkostěnná skleněná membrána, tvořící baničku na konci skleněné elektrody, je citlivá na H+ ionty. Při ponoření elektrody do měřeného roztoku dojde ke vzniku potenciálového rozdílu. Pokud bychom sledovali pouze potenciál měrné elektrody, nemůžeme určit pH roztoku. Pro určení je potřeba další elektroda, tzv. referenční elektroda. Pro stanovení je třeba rozdílný (diferenční) potenciál obou elektrod. Odezva měrné elektrody je závislá na koncentraci vodíkových iontů H+, čímž poskytuje informaci o kyselosti či zásaditosti roztoku. Naopak referenční elektroda tuto informaci neposkytuje. Referenční elektroda je zdrojem konstantního potenciálu, ke kterému se pak vztahuje potenciál měrné elektrody. Potenciál mezi dvěma elektrodami určuje množství vodíkových iontů H+, který pak definuje pH roztoku.
V případě tohoto úkolu se přesvědčíme o funkčnosti tlumivého roztoku v porovnání s hydroxidem o stejném počátečním pH +/- 10. Měření se provádí vždy po přidání 20 µl 5 % HCl.
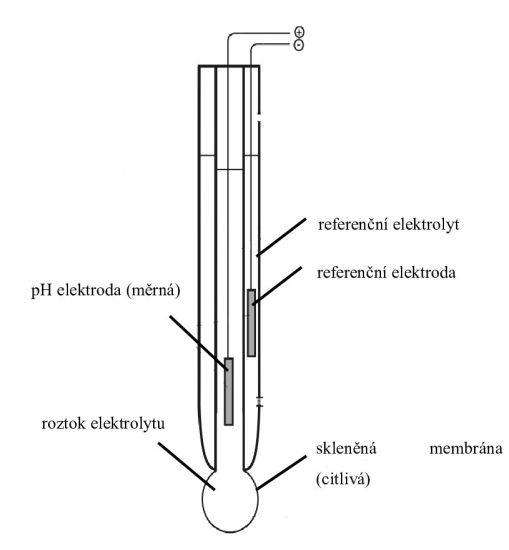
Obr. 1: Schéma kombinované skleněné elektrody.